Trial Clinici attivi contrastanti aggregazione proteine nella SLA: gli oligonucleotidi antisenso
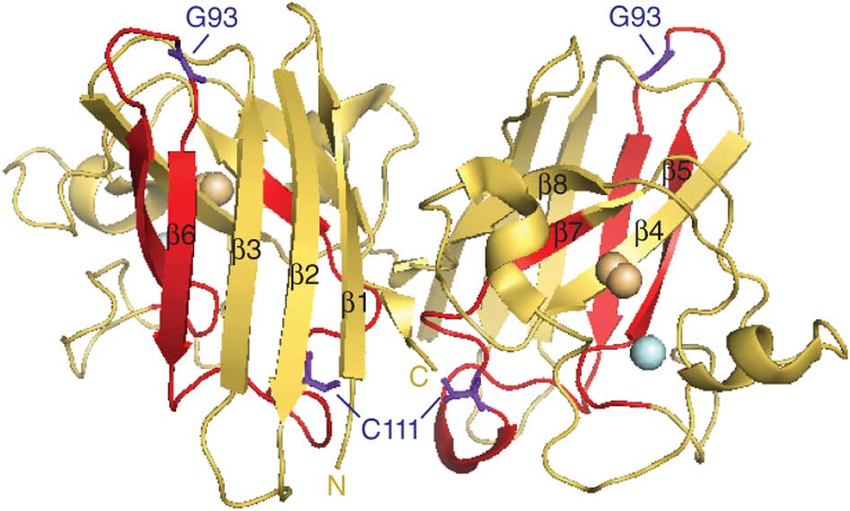
Le alterazioni strutturali (misfolding) della proteina SOD1 così come mutazioni del gene coinvolte in circa il 10% dei pazienti SLA,
contribuiscono all’insorgenza e alla progressione della malattia. L’utilizzo di anticorpi contro le forme alterate della proteina potrebbe essere un’ulteriore opzione terapeutica per la malattia sia per le forme familiari che sporadiche. Alcuni studi hanno riportato che il trattamento con anticorpi anti SOD1 è associato ad un miglioramento della sopravvivenza in modelli animali di SLA. Un’altra possibile strategia terapeutica consiste nell’uso di oligonucleotidi antisenso, brevi molecole complementari ad una determinata sequenza, utili a ridurre la sintesi delle proteine alterate o tossiche come SOD1 o C9ORF72, la più comune causa genetica di SLA. Questa strategia è già stata utilizzata per SOD1, sia in modelli preclinici, sia in studi clinici.
Un trial di fase I condotto negli USA, sponsorizzato da ISIS Pharmaceuticals (che è diventata IONIS Pharmaceuticals), con ISIS-SOD1RX in 33 pazienti familiari mutati per SOD1 è stato completato e la terapia, che ha previsto l’infusione nel canale spinale del farmaco, si è dimostrata sicura e ben tollerata (ClinicalTrials.gov Identifier: NCT01041222); non è stata riportata tossicità dose dipendente e nessun evento avverso serio è stato riportato nei pazienti in trattamento (Miller TM et al, 2013 Lancet Neurology).
A dicembre 2015 IONIS Pharmaceuticals ha annunciato una partnership con Biogen per un trial di fase I/IIa con ISIS-SOD1Rx (BIIB067) in 84 pazienti con SLA e SLA familiare SOD1 (ClinicalTrials.gov Identifier: NCT02623699). La Biogen sta conducendo il trial randomizzato, in doppio cieco, placebo-controllato con dosi differenti di oligonucleotide per valutare la sicurezza, la tollerabilità, la farmacocinetica e farmacodinamica con iniezioni intratecali. Lo studio è attualmente in fase di reclutamento ed è attivo in Stati Uniti, Canada, Francia, Germania, Belgio, Svezia e UK.
I primi risultati sono attesi la primavera/estate del 2018.
Per il trattamento della mutazione C9ORF72 sempre IONIS Pharmaceuticals e Biogen stanno sviluppando una potenziale strategia con oligonucleotidi antisenso. C’è l’intenzione di iniziare un trial clinico di fase I con lo scopo di rallentare la progressione della malattia nei pazienti C9orf72 riducendo i livelli di RNA potenzialmente tossico e, di conseguenza, riducendo i livelli di dipeptide tossico.
FONTE:









